성분 상세정보
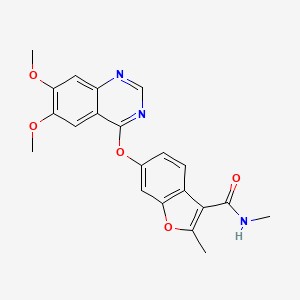
정보 수정요청| 성분명 | 프루퀸티닙 (Fruquintinib) |
분자식 : C21H19N3O5 분자량 : 393.4 g/mol from PubChem CID 44480399 |
|---|---|---|
| 동의어 |
|
|
| 작용기전 | 작용기전 및 약력학적 효과
이 약은 종양 혈관 생성을 억제하여 항종양 효과를 나타내는 혈관 내피 성장인자 수용체(VEGFR)-1, -2, -3의 선택적인 티로신 키나아제 억제제이다. 심장 전기생리학 이 약의 권장 용량 투여 시 심박수 보정 QT(QTc) 간격 연장(>10msec)은 관찰되지 않았다. 이 약의 혈장 농도와 기저 수준에서의 QTc 간격 변화 사이에 연관성은 정립되지 않았다. |
|
| 약동학 | 흡수
이 약의 경구투여 후, 최고혈중농도 도달시간(Tmax) 중앙값은 약 2시간이다. 1일 1회 반복 투여 후, 프루퀸티닙의 노출(Cmax 및 AUC0-24h)은 1 ? 6mg(권장용량의 0.2 - 1.2배) 용량 범위에서 용량 비례적으로 증가했다. 진행성 고형암 환자에서 28일 치료 주기에서 21일 동안 치료를 받은 후 7일 동안 휴약하는 방식으로 이 약 5mg을 1일 1회 투여한 결과, 14일 후에 항정상태에 도달하였고, 이 때 기하평균(%CV) Cmax 및 AUC는 각각 300ng/mL(28%) 및 5,880ng*h/mL(29%)이었다. AUC0-24h에 근거한 평균 축적은 단회투여에 비해 4배였다. 식이영향 공복 상태와 비교하여, 고지방 식사는 건강한 시험대상자에서 이 약의 약동학에 임상적으로 유의미한 영향을 미치지 않았다. 이 약은 음식과 함께 또는 공복 상태에서 투여가 가능하다. 분포 이 약의 겉보기 분포용적은 약 48.5 L이다. 시험관내(in vitro) 혈장단백결합률은 약 95%이다. 대사 이 약은 주로 CYP450(CYP3A 및 CYP2C 아형) 및 비-CYP450 효소 시스템으로 대사되며, 주로 인간 혈장에서 미변화체로 존재한다. 시험관내(in vitro) 시험 CYP 450 효소: 이 약은 CYP3A4에 의해 주로 대사되었고, CYP2C8, CYP2C9 및 CYP2C19의 영향은 미미하였다. 이 약은 치료적으로 유의미한 농도에서 CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 및 CYP3A의 억제제 또는 CYP1A2, CYP2B6, CYP3A의 유도제가 아니다. 수송체 시스템: 이 약은 P-gp, OATP1B1, 또는 OATP1B3의 기질이 아니다. 이 약은 치료적으로 유의미한 농도에서 OATP1B1, OATP1B3, OAT1, OAT3, OCT2, MATE1, 또는 MATE2-K의 억제제가 아니다. 배설 이 약의 평균 소실 반감기는 약 42시간이고 겉보기 청소율(CL/F)은 진행성 고형암 환자에서 항정상태에서 14.8mL/min이다. 건강한 시험대상자에서 방사성 동위원소로 표지된 이 약 5mg을 단회투여한 후, 투여용량의 약 60%는 소변(미변화 0.5%)에서, 30%는 대변(미변화 5%)에서 회수되었다. 특수 집단 연령, 체중, 성별 또는 인종 집단 약동학 분석에 따르면, 연령(18-82세), 체중(48-108 kg), 성별 또는 인종에 따른 이 약의 임상적으로 유의한 약동학적 차이는 없었다. 신장애 환자 집단 약동학 분석에 따르면, 경증 내지 중등도 신기능 장애(크레아티닌 청소율[CrCL]30 ~ 89mL/min)는 이 약의 약동학에 임상적으로 유의한 차이가 없었다. 약동학 시험에서, 정상 신기능(CrCL ≥ 90 mL/min, N=8) 시험대상자와 비교하여 중등도 신기능(CrCL 30-59 mL/min, N=8) 또는 중증 신기능(CrCL 15-29 mL/min, N=8) 시험대상자의 비결합 AUC0-inf 및 Cmax는 비슷하였다. 간장애 환자 집단 약동학 분석에 따르면, 정상 간기능 환자와 경증 간 장애(총 빌리루빈 ≤ULN 및 AST > ULN 또는 총 빌리루빈 >1 ~ 1.5X ULN 및 모든 수치의 AST) 환자 간에 이 약의 약동학에서 임상적으로 유의한 차이가 없었다. 약동학 시험에서, 이 약 2mg을 단회투여 시 정상 간기능 시험대상자 대비 중등도 간장애(Child PughB) 시험대상자의 dose-normalized AUC는 임상적으로 유의미한 차이는 없었다. |
※ 이상반응, 금기, 주의사항, 상호작용 등의 정보는 개별 의약품의 허가정보에서 확인하실 수 있습니다.